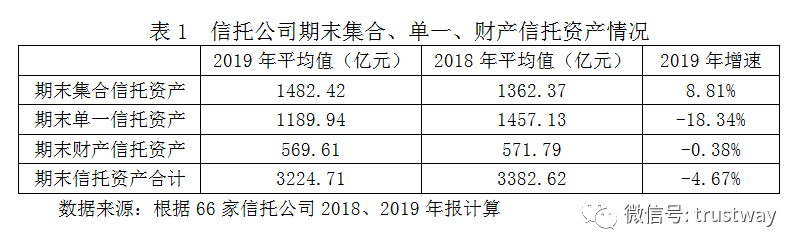
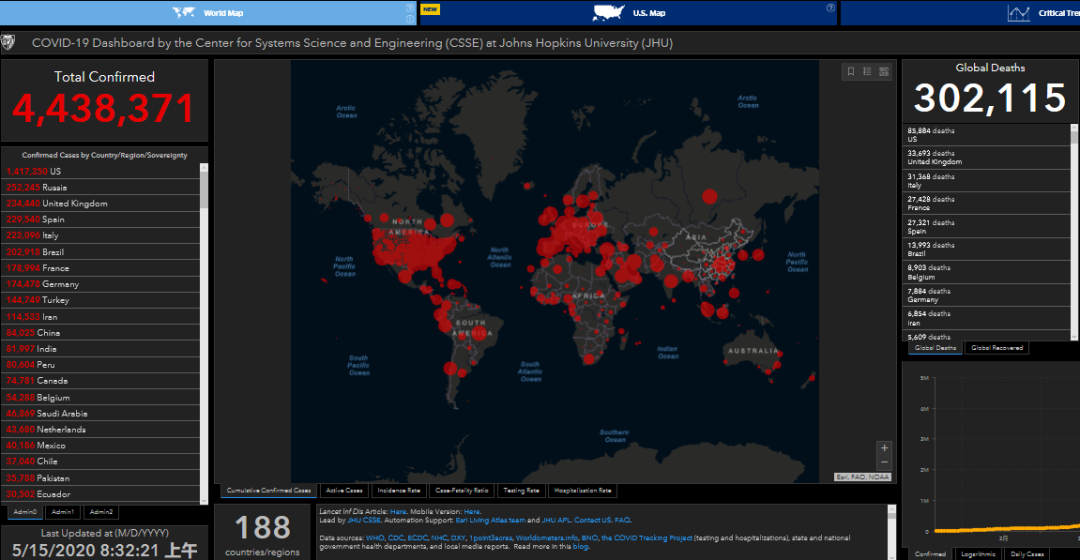
海关总署5月17日发布的数据显示,3月1日至5月16日,全国共验放出口防疫物资价值1344亿元。其中,新型冠状病毒检测试剂盒1.62亿人份。防疫物资主要出口目的地为美国、德国、日本、法国、意大利。据我们从欧洲专业杂志等获取的信息,东方生物的POCT快速新冠试剂在评测中获得了较高评价。
瑞典、法国、荷兰机构
认可东方生物检测试剂
上个月,瑞典权威医学杂志《Infection Ecology & Epidemiology》的一篇文献评估了东方生物POCT快速新冠试剂。
文中通过29例经PCR证实的COVID-19病例和124例阴性对照评估东方生物POCT快速新冠试剂,评估结果显示该试剂对IgM和IgG的灵敏度为69%、93.1%,对IgM和IgG的特异性达到100%、99.2%,研究显示该试剂快速检测的效果令人满意。
本文的研究者来自瑞典乌普萨拉大学人畜共患病科学中心医学生物化学和微生物学系、传染病研究室、临床微生物学研究室和临床科学研究室。乌普萨拉大学是国际顶尖的综合性大学。
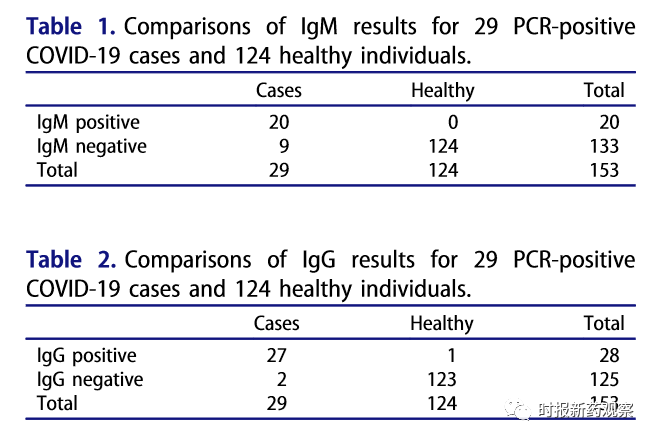
同样在4月份,荷兰最大的大学医学中心Erasmus MC 对3款新冠病毒快速抗体检测试剂进行了敏感性和特异性研究,3款产品分别是InTec Product公司的SARS-CoV-2快速抗体(IgM/IgG)检测、Cellex公司的qSARS-CoV-2 IgG/IgM盒式快速检测试剂(GICA)以及东方生物的COVID-19 IgG/IgM快速检测检测盒(全血/血清/血浆)。
根据PCR证实的COVID-19患者93份样本的检测结果,东方生物的COVID-19 IgG/IgM快速检测盒总敏感度为83.33%(74.94%-89.81%),特异性为100%(66.37%-100%)。症状出现7天后采集样本的敏感度为88.46%(79.22%~94.59%),特异性为100%(66.37%~100%)。在被评估的3个试剂中,东方生物的检测试剂总敏感度第二,特异性最高。

除此之外,法国的病毒学家也在评估东方生物的新冠病毒检测试剂的敏感性和特异性。这项研究计划包括至少100名COVID+患者来测量敏感性,50名COVID-患者来测量特异性。目前,已有42名COVID+患者和28名COVID-接受了检测。中期的研究结果显示,该试剂在无症状人群和14-21天以上症状人群的筛查表现令人满意。
综上可见,东方生物的POCT快速新冠试剂在欧洲受到了较高的质量评价,将有助于公司产品的出口。
东方生物两个新冠试剂进入出口白名单
4月26日,国家对新冠医疗物资出口实施白名单制度,进入白名单的产品才能出口。4月27日,在中国医药保健品进出口商会公布的首批白名单中,东方生物的一个已取得CE认证的新型冠状病毒检测试剂进入白名单。5月11日,中国医药保健品进出口商会更新的白名单中,东方生物允许出口的新型冠状病毒检测试剂增加到了两个。
东方生物是我国主要的POCT即时检测试剂生产商。据此前的公开信息,新冠肺炎发现后的1月份,东方生物即利用POCT检测试剂平台展开了相应检测试剂的研发,2、3月份开始将新冠POCT即时检测试剂出口至欧洲,并取得了欧盟CE认证。
4月1日,国家药监局叫停未通过国内注册的新冠检测试剂出口。东方生物是一家以出口为主的检测试剂生产企业,海外营收占公司业务收入的94%左右, POCT即时检测等两个新冠试剂也未在国内完成注册,叫停行为对公司的影响较大。进入白名单后,意味着东方生物的新冠POCT即时检测试剂5月份开始可以重新出口。
在疫苗未出来前,检测是防治新冠肺炎的重要工具。澳大利亚联邦政府周四证实,他们花了990万澳元从澳洲分销商MD Solutions购买了50万盒OnSite抗体测试盒,被发现灵敏度不足。5月初,印度有多个邦州反映中国试纸出现质量问题。上月,据美国媒体报道,美国疾病控制预防中心(CDC)生产的用于新冠肺炎检测的试剂不合格。在此背景下,获国际认可并形成良好声誉的新冠试剂未来更有可能收获更多订单。