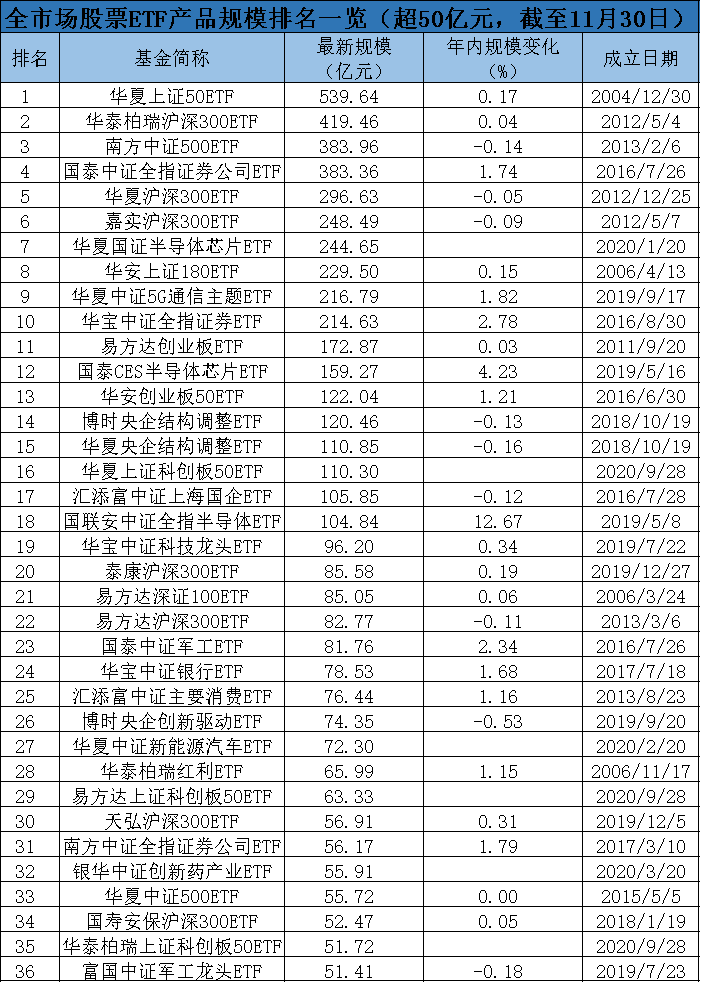
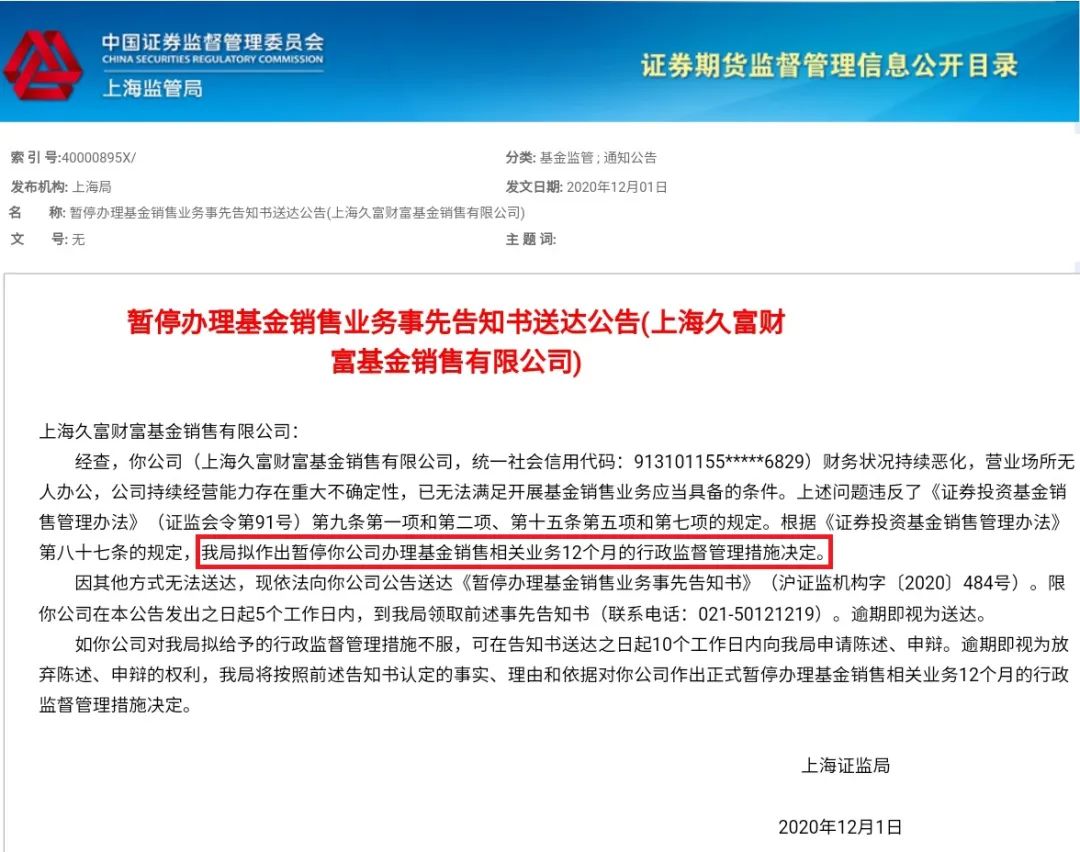
英美接连批准新冠疫苗交付时,我国新冠疫苗距离上市的脚步也近了。日前,孙春兰、王勇在京调研时指出,要做好新冠疫苗大规模生产准备。省级新冠疫苗采购工作也已开始,12月1日,江苏省正式开启了三款新冠疫苗的采购工作。
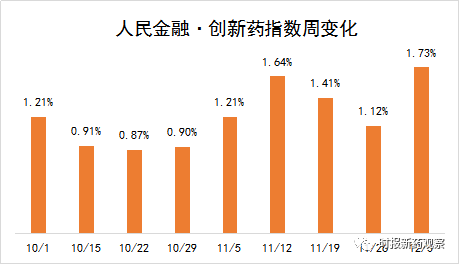
在11月27日至12月3日的发布周期内,方盛制药和一力制药各有一个1.1类中药的新药上市申请获受理,另外百济神州、石药集团、片仔癀、海思科等的9个创新药获批临床,我们将其纳入了“人民金融·创新药指数”。目前,“人民金融·创新药指数”的成分样本数共有670个。截至12月3日,“人民金融·创新药指数”报1265.13点,在最近一个发布周期内上涨了1.73%,涨幅创出近4个月新高。
省级新冠疫苗采购工作开启
全球新冠疫苗进入了最后的冲刺,英美接连批准新冠疫苗交付时,我国新冠疫苗距离上市的脚步也近了。
据新华社报道,12月2日,国务院副总理孙春兰、国务委员王勇在北京调研新冠病毒疫苗研发和生产准备工作。孙春兰指出,根据冬季疫情防控需要,今年完成口岸相关从业人员和一线监管人员等高风险人群的紧急使用工作。
孙春兰指出,下一步,要继续科学严谨推进疫苗Ⅲ期临床试验,严格按照法律法规和国际认可的技术标准做好审评审批工作,确保疫苗安全有效、经得起各方面检验。要做好大规模生产准备,严格按照质量监管、生物安全等法规、程序和要求,健全疫苗全流程追溯体系,依法严惩违法违规行为,营造良好市场环境。要研究制定疫苗上市后的接种分配方案,明确人群范围、接种顺序和时间考虑,提前组织疾控机构和基层接种单位的人员培训。
与此同时,省级新冠疫苗采购工作也悄然开展。12月1日,江苏省正式开启了三款新冠疫苗的采购工作。江苏省公共资源交易中心发布的《关于开展新型冠状病毒疫苗采购工作的通知》指出,为保障江苏省新冠疫情防控工作的需要,江苏省将进行三款新冠疫苗的采购工作。
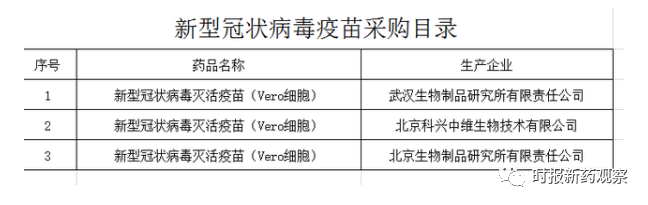
采购目录显示,江苏本次采购的新冠疫苗均为可紧急使用的新型冠状病毒灭活疫苗(Vero细胞),分别来自武汉生物制品研究所有限责任公司、北京科兴中维生物技术有限公司、北京生物制品研究所有限责任公司。此外,江苏此次即将开展的新冠疫苗采购还将进行价格谈判工作。
目前,我国五款新冠疫苗进入了三期临床,其中国药集团的进展最快,11月25日,国药集团副总经理石晟怡称,国药集团已向国家药监局提交了新冠疫苗上市申请。科兴中维的新冠疫苗进度紧随其后,11月28日,在2020首届中国卫生健康科技创新发展大会上,科兴控股生物技术有限公司董事长尹卫东表示,公司的新冠疫苗克尔来福在巴西开展的III期临床研究,预计将于12月初完成中期分析。
石药集团首创药获批临床
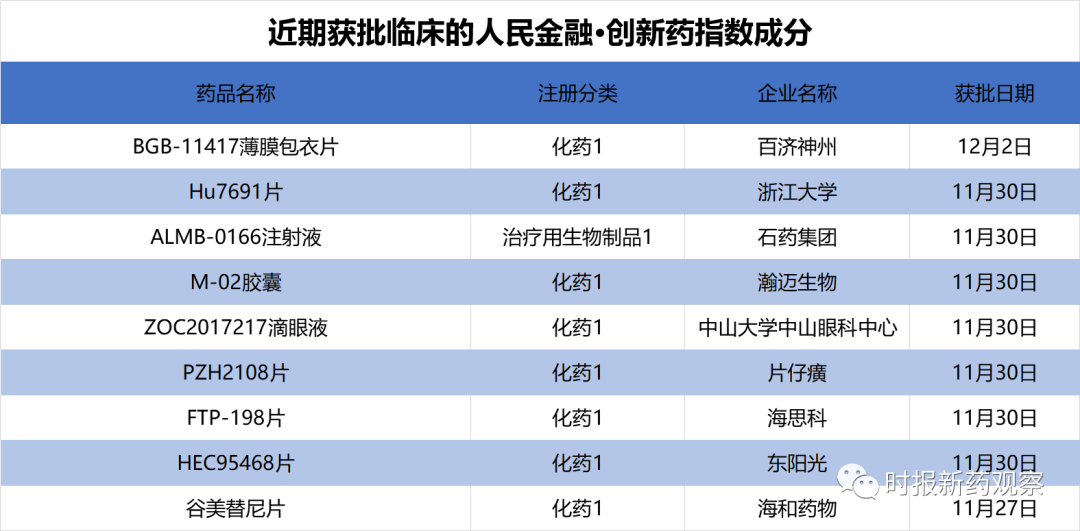
在11月27日至12月3日的发布周期内,来自百济神州、石药集团、片仔癀、海思科等药企的9个创新药获批临床,新发布周期内获批临床的创新药数量创新高。
其中,石药集团又一全球首创药获批临床。11月30日,石药集团附属公司上海恩乐迈生物科技有限公司的ALMB-0166获批临床,适应症为急性脊髓损伤。ALMB-0166为一款同类首创(first-in-class)针对全新靶点半通道膜蛋白Cx43的人源化单克隆抗体抑制剂,该药已于2018年获得美国FDA颁发用于治疗急性脊髓损伤的孤儿药资格认定,另针对该适应症在澳大利亚的I期临床试验已经完成给药,显示了优良的安全性和耐受性。
石药集团正在进行从“中国新”到“全球新”的全球化战略。9月份,石药集团首个同类首创生物药——Cx43靶点激动性抗体ALMB-0168获得国家药品监督管理局批准,可以在中国开展用于治疗骨癌和癌症骨转移的临床试验。目前,石药集团已有9产品在国外开展临床试验,恩必普软胶囊处于II期临床阶段;恩必普、抗体药物偶联物ADC等5个产品获得美国FDA颁发孤儿药的资格,并展开新药临床试验。
百济神州获批的属于潜在同类最佳创新药。12月2日,百济神州的BGB-11417薄膜包衣片获批临床,拟用于治疗成熟B细胞恶性肿瘤,这是该产品首次在中国申报临床。根据百济神州早前发布的公开资料,这是一款高选择性、潜在“best-in-class”的Bcl-2抑制剂。百济神州已在今年第一季度启动BGB-11417用于治疗成熟B细胞恶性肿瘤患者的1期临床试验,并计划将其作为单药以及联合BTK抑制剂泽布替尼进行开发。
目前,国内尚无Bcl-2抑制剂上市,进度最快的为艾伯维的维奈克拉片,已于11月进入行政审批阶段,亚盛医药的APG-1252和APG-2575片、复星医药的FCN-338片等针对BCL-2通路的在研品种已进入临床阶段。
继首个创新药于8月底取得临床批件后,11月30日片仔癀的PZH2108片也获国家药监局默认许可临床试验,用于治疗癌性疼痛。片仔癀称,PZH2108片是具有自主知识产权的化学药品1类创新药,国内外暂无相同适应症的同靶点药品获批上市。公司已经完成PZH2108片原料药以及制剂的药学、药理毒理、非临床安全性评价等方面的研究,研究结果表明PZH2108片具有良好的安全性、成药性及临床开发价值。该药品项目的研发投入累计约2800万元。
此外,近日东阳光的HEC95468片获批临床,拟开展适应症为治疗慢性心力衰竭、肺动脉高压(PAH)、慢性血栓栓塞性肺高血压(CTEPH),这是东阳光今年第7款获批临床的1类新药;天广实的创新型的II型抗CD20重组人源化单克隆抗体MIL62获批临床,用于治疗狼疮性肾炎;海思科的FTP-198片获批开展用于特发性肺纤维化的临床试验。
两个创新中药上市申请获受理
创新药审评审批进展和临床试验状态变化也是推动“人民金融·创新药指数”走高的原因。
在最新发布周期内,方盛制药的金古乐片和一力制药的虎贞清风胶囊两个1.1类中药新药上市申请获受理。方盛制药7月份曾公告,基于药物的组成、作用、药效学的研究以及Ⅱ、Ⅲ期临床试验结果,公司研发的金古乐片对于膝骨关节炎(筋脉瘀滞证)所致局部疼痛,关节僵硬,日常活动不利受限,局部肿胀,压痛等症状具有良好的改善作用;在试验过程中,试验药物不良反应发生率与安慰剂比较无明显差异,服用将安全。
事实上,近一个月来,创新中药的注册和审评审批取得了较大的突破,有3个1.1类中药新药上市申请获受理,来自江中药业和多灵生物的两个创新中药获批临床。这是今年以来,中药新药首次获批临床。
多个“人民金融·创新药指数”成分样本的临床试验向前推进。最近,众生药业登记启动了其ZSP1273片治疗成人单纯性甲型流感的Ⅲ期临床研究。ZSP1273片是国内首个获批临床试验的治疗甲型流感的小分子RNA聚合酶抑制剂。目前,国内尚未有同类一类创新药物正在开展用于治疗成人单纯性甲型流感的Ⅲ期临床研究登记,在同类药物临床研究中进展最快。若受试者招募顺利,三期临床有望于2021年年中获得结果。
另外,石药集团的SYHA1805片、复星医药的FCN-011胶囊、天广实的重组人源化单克隆抗体MIL95注射液等近期也登记启动了I期临床。